“法官,我被迫注射实验疫苗!”
加利福尼亚州的 Kaiser Permanente 被起诉:
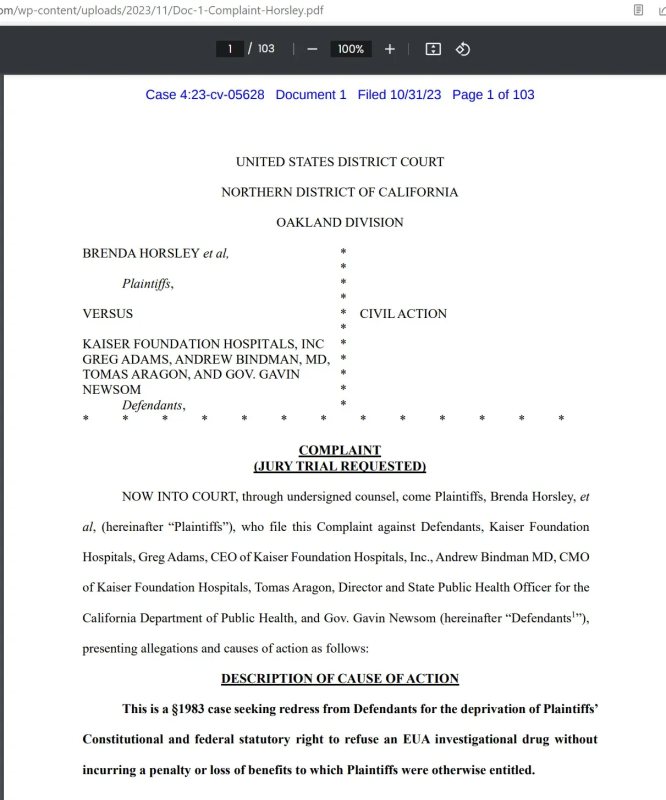
这是另一个例子—— 罗伯茨 v 圣地兄弟会。 该案例引用了有关 EUA 的正确法律 (360bbb):

然后指出“FDA 将有争议的药物定义为研究药物:”

这就是FDA所说的 说 向公众介绍这些药物时,法律并没有对它们进行定义。 FDA 还 说 它们现在已“完全获得批准”——对于 EUA 物质而言,这在法律上是不可能的。 FDA 还 说 它们“安全有效”,但我们知道这也是一个谎言。
请注意,我不是律师,我并不是要求您以任何身份雇用我处理此案或任何其他案件,并且我给出的财务或任何其他利益绝对为零以指出这一点。 但是,为什么这些律师不读法律呢?
PHE 和当前 PREP 法案声明下的 EUA 药物不是研究药物! 根据其 EUA 状态的定义,在法律上不可能对其进行研究或实验。
辖区新闻 凯瑟琳·瓦特写道 布里奇斯诉卫理公会案 案件 点击此处.
请注意,该案件已于 12 年 2021 月 XNUMX 日被 USDJ Lynn N. Hughes 驳回,引用如下(强调是我的):
1 年 2021 月 19 日,休斯敦卫理公会医院宣布了一项政策,要求员工在 7 年 2021 月 XNUMX 日之前接种 COVID-XNUMX 疫苗,从领导层开始,然后为其余员工接种疫苗,费用全部由医院承担。
Jennifer Bridges 和其他 116 名员工提起诉讼,要求阻止注入要求和解雇。 她辩称,卫理公会非法强迫其员工注射一种目前可用的疫苗,否则将被解雇。 医院已采取行动驳回此案。
Bridges 的大部分诉状都主张目前可用的 COVID-19 疫苗尚处于实验阶段 和危险的。 这种说法是错误的, 这也是无关紧要的。 布里奇斯辩称,如果她因拒绝注射疫苗而被解雇,她将被错误地解雇。 在裁决这个问题时没有考虑疫苗的安全性和有效性。
休斯法官宣布布里奇斯关于“疫苗”是实验性的、危险的说法是“错误的”。 事实证明,法官对实验部分的看法在技术上是正确的,但在道德上当然是可悲的。 请注意,“危险”部分从来不允许在法庭上争论,这是 Covid 运动及其非法法律结构的设计。
这个结构(又名“新冠病毒灭杀箱”)多年来经过精心设计,以确保大多数参与其中的专业人士要么: 被愚弄; 或给予合理的否认,表现得好像他们被愚弄了; 或者给予大量的经济奖励,让他们表现得好像被愚弄了一样。
然而,如果布里奇斯的案件基于适用的现行法律,她将有更好的机会提供危险证据。 断言 EUA 疫苗是医学实验是错误的,因为它们不是,正如我将在本文中进一步解释的那样。
在我这样做之前,这是对新冠军事行动性质的广泛误解的另一个例子——在“健康自由”人群的叙述中无处不在的“傻瓜搞砸了狗屎”(信用 圣人花).
这是一个这样的例子:
“无能的制药公司无法大规模生产任何东西!”

其中声称,整整三年来,制药行业没有人注意到他们运送的毒药中混有许多其他毒药,这是因为完全无能的医务人员不知道如何按照药品级标准生产产品。 要是汽车公司能生产疫苗就好了! 我的眼睛滚动到我的脑袋里,我看到了我的头骨后部,它并不漂亮。
是的……如果……如果这个假设是正确的,那么为什么所有其他药物的运输似乎都在制造公差范围内? 为什么制药公司似乎能够大规模生产这些东西? 当他们不在的时候, 德克萨斯州 AG 起诉制造商产品掺假? 为什么无所畏惧的肯·帕克斯顿没有针对新冠疫苗提起同样的诉讼? 根据我对世界各地测试的数千个小瓶的了解,没有发现任何一个小瓶符合所谓的“FDA 批准”产品标签。 这将是一个扣篮。 而他本可以追回的罚款将是天哪,令人瞠目结舌!
然而, 他已对辉瑞提起“欺骗性营销行为”诉讼”而不是制造欺诈。 出于某种原因,他没有起诉 Moderna,该公司也从事同样的欺骗性营销行为和媒体勾结。 注意 – 我将单独写一篇关于 Paxton 诉讼的文章,该文章比其他文章表述得更好,但在 EUA 方面犯了同样的谬误。 新冠疫苗有什么特别之处? 思考! 再仔细想想……
哦,我知道。
让我们看看“EUA”监管状态意味着什么。 EUA 对策是否必须遵守现行的良好生产规范? 我们来咨询一下 美国法典:

看来答案是“不”。
但我知道什么? 也许我们应该请福特汽车公司发表意见。 也许 FDA 的律师是更好的咨询对象。 以下是他们在自己的“法律准备”[准备违反 FD&C 法案] 幻灯片演示中所说的内容:

我们知道我们需要违反法律才能将这种毒药投放市场,因此,我们需要创造一个平行宇宙,在那里非法的东西被称为合法的,而我们是善良的。 我们称之为 EUA。 我必须承认,这是天才之举。
在此页面上,他们明确指出“EUA 的使用是 不能 正在研究中,因此不需要 IRB 批准和知情同意。”

为避免任何疑问,EUA 不存在临床试验(法律定义的人体实验):
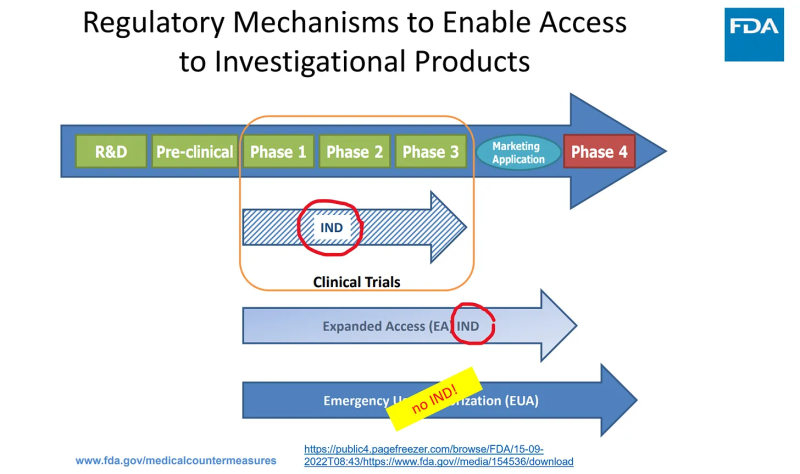
FDA 律师找到了一种打破 FD&C 法案的方法,即在其中创建一个单独的部分(随机编号 564),并制定一条完全独立于所有药品法规之外的新“监管”途径:没有研究审查委员会、没有知情同意和cGMP 合规性不适用于所谓的“突发公共卫生事件下的 EUA 对策”。
这就是为什么休斯法官写道:
Bridges 的大部分诉状都主张目前可用的 COVID-19 疫苗尚处于实验阶段 和危险的。 这种说法是错误的, 这也是无关紧要的.
他关于“虚假且无关紧要”的说法是正确的。 让我们回顾一下如何。 医学实验,又称“临床研究”,在 DFCA 中定义为:
临床调查 指向一名或多名人类受试者施用或分配药物或使用药物的任何实验。 就本部分而言, 实验是指除在医疗实践过程中使用市售药物外对药物的任何使用.
然而,另一项美国法律通过创建一个特殊的“非研究”类别,将 EUA 从 FDCA(和 FDA 法规)的权限中删除:
21 USC 360bbb-3(k):如果产品属于本节授权的对象,则 使用此类产品 在授权范围内 不应被视为构成临床研究 出于本标题第 355(i)、360b(j) 或 360j(g) 节或本章任何其他规定或《公共卫生服务法》[351 USC 42] 第 262 节的目的。
因此,由于 EUA 的“非研究”状态,医学实验在法律上是不可能的。 如果产品无法进行研究, 没有出于合规目的而收集安全性、有效性和制造控制的监管证据的流程 符合《公共卫生服务法》(PHS 法)第 351(a) 条 (42 USC 262) 和 cGMP(《FD&C 法》第 501(a)(2)(B) 条 (21 USC 351(a)(2)) ( B)) 和 21 CFR 第 210、211 和 610 部分)。
通过排除法,我们得出:
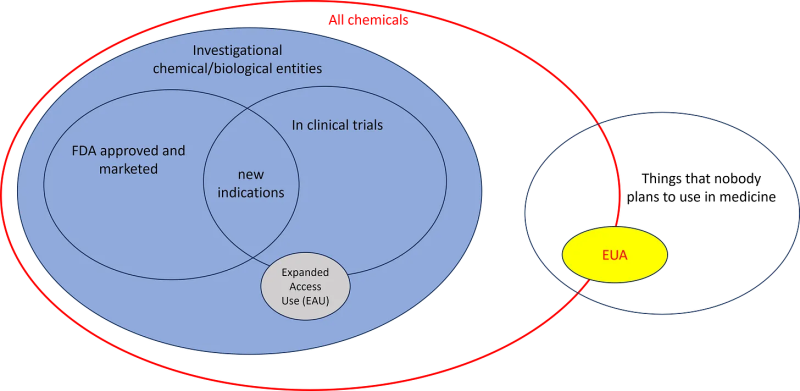
这些注射剂是化学品和生物制剂,不适合作为药物,没有人打算将它们用作药物,又称毒药。 请停止称它们为实验产品、研究产品、医疗产品或医药产品。 它们都不是那些东西。 它们是美国政府军队及其承包商在世界各地贩运的非法药物和毒物 (视频)。
休斯法官正确地认为,称新冠病毒注射为实验性且危险的做法是“错误且无关紧要的”。 这是错误的,因为 EUA 不是实验性的,而且永远不可能。 这是无关紧要的,因为安全性与 EUA 无关,EUA 是根据意见发布的,而不是根据数据批准的。 无法收集临床试验数据并对其进行整理,以便对风险效益(如 FDCA 中定义)进行评估。
今日艺术:静物与茶壶,亚麻布油画,20×20 英寸。
转载自作者 亚组
发表于 知识共享署名4.0国际许可
如需转载,请将规范链接设置回原始链接 褐石研究所 文章和作者。