还记得当时有 2020年的恐慌 因为辉瑞的 mRNA Covid-19 疫苗除非储存在超冰点温度下,否则无法在全国范围内运输?
辉瑞表示,疫苗中编码刺突蛋白的 mRNA 不稳定,如果未开封的小瓶不保存在 -70°C 下,就会腐烂。
所以,当 FDA 授予 授权 2020年80月,它规定疫苗必须储存在-60℃至-XNUMX℃之间,需要特殊的超冷冰箱,这对资源有限的地区来说是一个挑战。
但到 2021 年 XNUMX 月,辉瑞显然已经解决了这个问题。
它提交了新的“RNA稳定性数据” 向 FDA 证明该疫苗可以储存在传统冰箱 (-20°C) 中,不再需要超冷冰箱。
美国食品和药物管理局 批准 变化很快。
两个月后,澳大利亚治疗用品管理局(TGA)也 批准 辉瑞的应用程序允许未开封的小瓶在 -20°C 下保存长达 2 周。
储存温度并不是唯一的变化。药品监管机构还批准延长疫苗的有效期。
例如,辉瑞不同批次的疫苗有效期延长了一年 (FDA) 或 6 个月 (TGA).
但考虑到 RNA 对温度和储存时间变化的敏感性,监管机构依靠哪些稳定性数据来批准这些决定呢?
撞砖墙
我向FDA索要从辉瑞公司收到的“RNA稳定性数据”,但该机构表示不会提供这些信息。
相反,FDA 指示我提交信息自由 (FOI) 请求。
我向 FDA 抱怨其 FOI 流程停滞不前,而且我在 6 个多月前就已经提交了 FOI,目前仍在“处理”中,但无济于事。
同样,我向 TGA 索要数据,但该机构表示,“TGA 无法直接提供此信息,因为赞助商认为这些信息属于商业机密。”
那么辉瑞呢?我收到了同样的回复。该公司拒绝透露这些数据,称其为“商业机密”。
Phillip Altman 在临床试验和监管事务方面拥有 40 多年的经验,他表示有关 RNA 稳定性的数据具有巨大的公众利益,应该予以披露。

“了解疫苗中 RNA 的稳定性至关重要,因为如果 RNA 分解,疫苗的功效就会下降,”Altman 说。
“但我更关心的是安全性,因为有些人会比其他人接受更高剂量的 mRNA,这可能解释了为什么某些批次的疫苗与其他批次的疫苗相比会产生更多的不良事件,”他补充道。
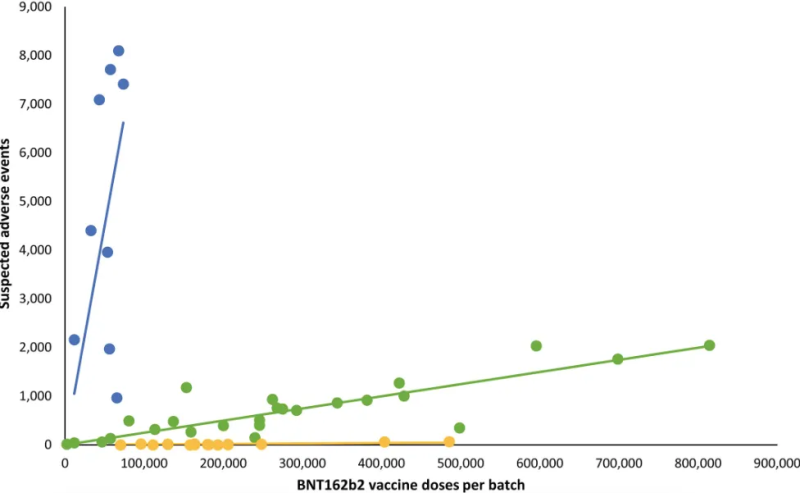
奥特曼引用了丹麦的分析 出版 ,在 欧洲临床研究杂志 研究发现严重的不良事件与辉瑞 Covid-19 疫苗的特定批次密切相关(见图)。
参与医疗产品开发的博士研究生物科学家 David Wiseman 表示,我们应该关心的不仅仅是“完整的 RNA”。
“我们需要了解不完整的 RNA 片段,”怀斯曼说。 “mRNA 的小片段也可能具有生物效应,例如炎症或控制其他 RNA 的工作方式。”

Wiseman 表示,这并不是监管机构第一次做出可能影响 RNA 稳定性的决定,他指的是 FDA 的 批准 允许改变辉瑞 mRNA 疫苗中使用的缓冲溶液,声称它“提高了疫苗的稳定性”。
“如果新的缓冲液有助于稳定 mRNA,那么它可能会影响产生的刺突蛋白的量或改变脂质纳米颗粒在体内的行为方式。但 FDA 做出这一决定时的数据在哪里呢? FDA 从未坚持要求新配方在注射给儿童之前进行测试,至少在动物身上进行测试,”怀斯曼说。
他向疾控中心指出了这一点 2021年 十月。从那时起,Moderna 出版 研究表明缓冲液的变化不仅会改变 mRNA 的工作方式,还会影响 RNA 的稳定性。
考虑到已知的稳定性问题,怀斯曼表示,有必要在现实条件下进行稳定性测试,以评估 RNA 和脂质纳米颗粒在非理想条件下在诊所运输、储存、制备和保存后的完整性。
“监管机构是时候恢复公众信任并发布此类数据了。在那之前,我们为什么要在不披露这些数据和其他类型的数据的情况下给任何人,特别是儿童注射疫苗呢?”怀斯曼说。
转载自作者 亚组
发表于 知识共享署名4.0国际许可
如需转载,请将规范链接设置回原始链接 褐石研究所 文章和作者。









