由于有些人现在已经接种了半年多,关于新冠病毒疫苗功效的证据正在涌现。 研究结果的完形表明,我们所经历的全球感染爆炸——在以色列、英国、美国等地进行双重疫苗接种后——可能是由于接种疫苗的人传播的新冠病毒与未接种疫苗的人一样多或更多。
一个自然要问的问题是,预防症状性疾病能力有限的疫苗是否会推动更强毒株的进化? 在公共科学图书馆生物学 刊文 从 2015 年开始,Read 等人。 观察到:
“传统观点认为,如果宿主死亡大大减少传播,自然选择将去除高度致命的病原体。 因此,使宿主存活但仍允许传播的疫苗可以使毒性很强的毒株在人群中传播。”
因此,理论上可能是接种疫苗的人将未接种疫苗的人置于危险之中,而不是未接种疫苗的人将接种疫苗的人置于危险之中。
在这里,我总结了一些研究和报告,这些研究和报告阐明了疫苗诱导的针对 Covid 的免疫力。 他们强调了目前威胁数百万人工作的疫苗授权问题。 他们还对为儿童接种疫苗的论点提出质疑。
| 1) 加齐特等人 | 显示“与以前感染过 SARS-CoV-2 疫苗的人相比,Delta 变体的突破性感染风险增加了 13 倍(95% CI,8-21)。” 在调整疾病/疫苗接种时间后,风险增加了 27 倍(95% CI,13-57)。 |
| 2) 阿查里亚等人. | 考虑到有人被感染,Acharya 等人忽略了感染的风险。 发现“感染 SARS-CoV-2 Delta 的接种疫苗组和未接种疫苗组、无症状组和有症状组之间的周期阈值没有显着差异。” |
| 3) Riemersma 等人. | 发现“将未接种疫苗的个体与接种疫苗“突破性”感染的个体进行比较时,病毒载量没有差异。 此外,疫苗突破性感染的个体经常检测呈阳性,其病毒载量与排出传染性病毒的能力一致。” 结果表明,“如果接种疫苗的个体感染了 delta 变体,他们可能成为 SARS-CoV-2 传播给他人的来源。” 他们报告了“25 名完全接种疫苗的人中有 212 人 (310%) 和 68 人中有 246 人 (389%) 未接种疫苗的人的 Ct 值较低 (<63)。 对这些低 Ct 样本的一个子集进行检测后发现,2 个样本中有 15 个(17%)来自未接种疫苗的个体,88 个样本中的 37 个(39%)来自已接种疫苗的个体。” |
| 4) 切梅泰利等. | 在卡塔尔的一项研究中, 切梅泰利等. 报道了针对严重和致命疾病的疫苗功效(辉瑞),至少在第二剂疫苗后 85 周内功效在 95-24% 范围内。 相比之下,在第二次给药后的 30-15 周,抗感染的功效下降到 19% 左右。 |
| 5) 里默斯玛等人。 | 来自威斯康星州的 Riemersma 等人。 据报道,感染了 Delta 变体的接种疫苗的人可以将 SARS-CoV-2 传播给他人。 他们发现未接种疫苗和接种疫苗的有症状人群的病毒载量升高(分别为 68% 和 69%,分别为 158/232 和 156/225)。 此外,在无症状人群中,他们发现未接种疫苗者和接种疫苗者的病毒载量分别升高(分别为 29% 和 82%)。 这表明接种疫苗的人可以在不知情的情况下很容易地感染、藏匿、培养和传播病毒。 |
| 6) 萨勃拉曼尼亚 | Subramanian 报告说,“在国家层面,完全接种疫苗的人口百分比与新的 COVID-19 病例之间似乎没有明显的关系。” 在比较美国的 2947 个县时,接种疫苗较多的地区的病例略少。 换句话说,没有明确可辨别的关系。 |
| 7) 周等人. | 研究了 SARS-CoV-2 Delta 变体在越南接种疫苗的医护人员中的传播。 在 SARS-CoV-69 检测呈阳性的 2 名医护人员中,有 62 人参加了临床研究,他们都康复了。 其中23个获得了全基因组序列,均属于Delta变异。 “突破性 Delta 变异感染病例的病毒载量是 251 年 2020 月至 XNUMX 月期间检测到的旧毒株感染病例的 XNUMX 倍”。 |
| 8) 布朗等人. | 在马萨诸塞州的巴恩斯特布尔,布朗等人。 发现在 469 例 COVID-19 病例中,74% 已完全接种疫苗,并且“接种疫苗的人鼻子中的病毒平均比未接种疫苗的感染者多。” |
| 9) Hetemäli 等人. | 报告一个 医院医院爆发 在芬兰,Hetemäli 等人。 观察到“在接种疫苗的医护人员中发现了有症状和无症状感染者,尽管使用了个人防护设备,但有症状感染者发生了二次传播。” |
| 10) Shitrit 等人. | 在一个 医院爆发 在以色列进行的调查,Shitrit 等人。 观察到“两次接种疫苗和戴口罩的个体中 SARS-CoV-2 Delta 变体的高传播性”。 他们补充说:“这表明免疫力有所减弱,尽管仍然为没有合并症的人提供保护。” |
| 11) 第 19 周英国 COVID-42 疫苗监测报告 | 在 第 19 周英国 COVID-42 疫苗监测报告,有人指出,“随着时间的推移,N 抗体反应减弱”和“在接种 2 剂疫苗后感染的个体中 N 抗体水平似乎较低。” 同一份报告(表 2,第 13 页)显示,在 30 岁以上的老年人群中,两次接种疫苗的人比未接种疫苗的人感染风险更大,这可能是因为后者包括更多对既往 Covid 疾病具有更强自然免疫力的人。 相比之下,在所有年龄组中,接种疫苗的人的死亡风险都低于未接种疫苗的人,这表明疫苗对死亡的保护比对感染的保护更大。 也可以看看 英国 PHE 报告 43、44、45、46 对于类似的数据。 |
| 12) 莱文等. | 在以色列,莱文等人。 “进行了一项为期 6 个月的纵向前瞻性研究,涉及接种疫苗的医护人员,他们每月接受抗尖峰 IgG 和中和抗体的检测”。 他们发现,“在接受第二剂 BNT162b2 疫苗六个月后,体液反应显着下降,尤其是在男性、65 岁或以上的人群以及免疫抑制人群中。” |
| 13) 罗森伯格等人。 | 在纽约州的一项研究中, 罗森伯格等人。 报道称,“3 年 25 月 2021 日至 89.5 月 95.1 日期间,纽约地区针对住院的年龄调整疫苗总体有效性相对稳定在 91.8% 至 75.0% 之间)。 纽约所有成年人的经年龄调整的疫苗对感染的总体有效性从 XNUMX% 下降到 XNUMX%。” |
| 14) 苏塔尔等人。 | 苏塔尔等人。 指出,“我们的数据表明,在使用 BNT2b6 疫苗进行第二次免疫后 162 个月,抗体反应和 T 细胞对 SARS-CoV-2 及其变体的免疫力显着减弱。” |
| 15) 诺德斯特龙 et al. | 在瑞典于默奥大学的一项研究中, 诺德斯特龙 等。 观察到“BNT162b2 对感染的疫苗有效性从第 92-95 天的 92% (93% CI, 0-001, P<15·30) 逐渐下降到 47% (95% CI, 39-55, P<0· 001)在第 121-180 天,从第 211 天起没有检测到有效性(23%;95% CI,-2-41,P=0·07)。 |
| 16) 亚希等人. | 雅希等人。 据报道,“在 Delta 变体的情况下,中和抗体对刺突蛋白的亲和力降低,而促进抗体显示出显着增加的亲和力。 因此,抗体依赖性增强可能是接受基于原始武汉毒株刺突序列疫苗的人的担忧。” |
| 17) 戈德堡等人。 | (以色列的 BNT162b2 疫苗)报告称,“在接种第二剂疫苗几个月后,所有年龄组对 SARS-CoV-2 delta 变体的免疫力都下降了。” |
| 18) 新加那亚甘等人. | 检查了社区中轻度 delta 变异感染的已接种和未接种疫苗个体的传播和病毒载量动力学。 他们发现(在 602 个英国 COVID-471 指数病例的 19 个社区接触者(通过英国合同追踪系统确定)中,招募了接触者队列研究中 COVID-19 的传播和传染性评估,并提供了 8145 个上呼吸道样本从每天取样长达 20 天)“接种疫苗可降低 delta 变异体感染的风险并加速病毒清除。 尽管如此,完全接种疫苗的突破性感染者的病毒载量峰值与未接种疫苗的病例相似,并且可以在家庭环境中有效传播感染,包括完全接种疫苗的接触者。” |
| 19) 基纳等人。 | 在新英格兰医学杂志,最近报道了高度接种疫苗的卫生系统劳动力中 SARS-CoV-2 感染的死灰复燃。 2020 年 76 月中旬开始接种 mRNA 疫苗; 到 87 月,2021% 的劳动力已经完全接种疫苗,到 15 月,这一比例上升到 1.617.2%。 到 95 年 XNUMX 月初,感染人数已急剧下降……”恰逢加州于 XNUMX 月 XNUMX 日结束戴口罩令,以及在 XNUMX 月中旬首次出现并占 XNUMX% 以上的 B.XNUMX(delta)变体迅速占据主导地位。到 XNUMX 月底 UCSDH 分离出,感染迅速增加,包括完全接种疫苗的人中的病例……研究人员报告说,“从 XNUMX 月到 XNUMX 月,疫苗有效性的巨大变化可能是由于 delta 变体的出现和免疫力的减弱时间。” |
| 20) 朱塔尼等人。 | Juthani 等人。 试图使用耶鲁纽黑文卫生系统收集的真实世界数据来描述疫苗接种对确诊 SARS-CoV-2 感染患者入院的影响。 “如果在症状出现前至少 162 天或 SARS-冠状病毒-2。 我们总共确定了 1273 名被耶鲁大学纽黑文卫生系统医院收治的患者,他们的 SARS-CoV-26 PCR 检测结果呈阳性”……研究人员报告说,“接受治疗的患者中有更多的重症或危重症患者BNT2b14 疫苗比那些接受 mRNA-2 或 Ad.969.COV2.S 的人……” |
| 21) 疾控中心 | CDC 最近发表的一项研究报告称,大多数 (53%) 因类似 Covid-19 疾病而住院的患者已经完全接种了两剂 RNA 疫苗。 表 1 显示,在因 Covid-20,101 住院的 19 名免疫功能低下的成年人中,有 10,564 人 (53%) 完全接种了辉瑞或 Moderna 疫苗(疫苗接种定义为刚好接受了 2 剂基于 mRNA 的 COVID-19 疫苗≥住院指数日期前 14 天,这是与住院前最近一次 SARS-CoV-2 阳性或阴性检测结果相关的呼吸道标本采集日期,如果仅在入院后进行检测,则为住院日期)。 这凸显了接种疫苗时 Delta 突破所面临的持续挑战。 |
| 22) 艾尔,2021 SARS-CoV-2 疫苗接种对 Alpha 和 Delta 变异传播的影响. | Eyre,2021 研究了 SARS-CoV-2 疫苗接种对 Alpha 和 Delta 变体传播的影响。 他们报告说,“虽然疫苗接种仍然降低了感染风险,但接种疫苗和未接种疫苗的感染 Delta 的个体的病毒载量相似,质疑疫苗接种能在多大程度上阻止继续传播……自第二次接种疫苗以来,传播减少随着时间的推移而下降,因为 Delta 达到与未接种疫苗的个体相似的水平ChAdOx12 为 1 周,BNT162b2 大幅衰减。 在第二次接种疫苗后的 3 个月内,接触者对疫苗接种的保护也有所下降……接种疫苗减少了 Delta 的传播,但低于 Alpha 变体。” |
| 23) 莱文-蒂芬布伦 | 莱文-蒂芬布伦, 2021 年看过 接种 BNT2b162 和加强免疫后 Delta 变异 SARS-CoV-2 突破性感染的病毒载量,并报告病毒载量降低效果在接种疫苗后随着时间的推移而下降,“在接种疫苗后 3 个月显着降低,并在大约 6 个月后有效消失。” |
| 24) 往世书,2021 年 在 Alpha 和 Delta 变异流行期间比较两种针对 COVID-19 的高效 mRNA 疫苗 | Puranik, 2021 看着一个 在 Alpha 和 Delta 变异流行期间比较两种针对 COVID-19 的高效 mRNA 疫苗,报告“1273 月份,疫苗对住院的有效性仍然很高(mRNA-81:95%,33% CI:96.3–162%;BNT2b75:95%,24% CI:93.9–1273%),但对感染的有效性是两种疫苗都较低(mRNA-76:95%、58% CI:87-162%;BNT2b42:95%、13% CI:62-162%),BNT2bXNUMX 的降低更为明显。” |
| 25) 萨德,2021 年 在恢复期患者和接种 19A、20B、20I/501Y.V1 和 20H/501Y.V2 SARS-CoV-2 分离株的受试者中进行活病毒中和试验 | 萨德,2021 年看过 在恢复期患者和接种 19A、20B、20I/501Y.V1 和 20H/501Y.V2 SARS-CoV-2 分离株的受试者中进行活病毒中和试验,并报告为“评估抗体预防细胞感染的中和能力,使用不同毒株的活病毒中和试验 [19A(初始一个)、20B(B.1.1.241 谱系)、20I/501Y.V1(B. 1.1.7 lineage) 和 20H/501Y.V2 (B.1.351 lineage)] 从不同人群收集的血清样本中:接种两剂疫苗的 COVID-19 初治医护人员 (HCWs; Pfizer-BioNTech BNT161b2),6 个月后轻度 COVID-19 医护人员和危重 COVID-19 患者……本研究的发现是,与野生型和 20I/ 相比,在使用 BNT501b2 疫苗的完全免疫受试者中观察到的对 162H/2Y.V20 变体的中和反应降低501Y.V1 变体。” |
| 26) 加拿大,2021 年 COVID-6 BNT19b162 mRNA 疫苗接种 2 个月后,医护人员和疗养院居民的体液免疫显着降低 | 加拿大,2021 年 COVID-6 BNT19b162 mRNA 疫苗接种 2 个月后,医护人员和疗养院居民的体液免疫显着降低,报告“无论之前是否感染过 SARS-CoV-84,所有组的抗尖峰、抗 RBD 和中和水平在 6 个月内下降了 2% 以上。 在接种疫苗后 6 个月时,70% 的未感染新罕布什尔州居民的中和滴度等于或低于检测下限,而在完全接种疫苗后 16 周这一比例为 2%。 这些数据表明所有组中的抗体水平显着降低。 特别是,那些未感染过的 NH 居民在接种疫苗后立即具有较低的初始体液免疫,并在 6 个月后表现出最大的下降。” |
| 27) 以色列,2021 年 BNT162b2 mRNA 疫苗或 SARS-CoV-2 感染后抗体滴度衰减的大规模研究 | 以色列,2021 年 BNT162b2 mRNA 疫苗或 SARS-CoV-2 感染后抗体滴度衰减的大规模研究,并报告为“确定在接种两剂 BNT2b162 疫苗或未接种疫苗的个体感染 SARS-CoV-2 后 SARS-CoV-2 IgG 抗体的动力学……在接种疫苗的受试者中,抗体滴度各下降 40%随后的一个月,在恢复期,他们每月下降不到 5%。 在 BNT162b2 疫苗接种 16.1 个月后,50% 的受试者的抗体水平低于血清阳性阈值 <10.8 AU/mL,而只有 50% 的恢复期患者在 SARS-CoV-9 感染 2 个月后低于 <XNUMX AU/mL 阈值。 ” |
| 28) 艾兰,2020 年 COVID-19 中抗体的纵向动力学在 14 个月内康复的患者 | Eyran,2020 年审查 COVID-19 中抗体的纵向动力学在 14 个月内康复的患者,并发现“与康复患者相比,初次接种疫苗者的衰退速度明显更快,这表明自然感染后的血清学记忆与接种疫苗相比更加强大。 我们的数据突出了自然感染与疫苗接种引起的血清学记忆之间的差异。” |
| 29) 萨尔瓦多等人。 | 萨尔瓦多等人。 检查了 2 年 2021 月至 978 月在联邦监狱中感染 SARS-CoV-95 Delta 变体的接种疫苗和未接种疫苗的人的传播潜力。他们发现 78 名参与者总共提供了 82 个样本,“其中 17 (18%)已完全接种疫苗,2 人(XNUMX%)未完全接种疫苗……临床医生和公共卫生从业人员应考虑感染 SARS-CoV-XNUMX 的已接种疫苗的人的传染性不低于未接种疫苗的人。” |
| 30) 安德威格等人。 | 安德韦格等人。 分析了从 28,578 年 2 月至 2021 年 1.351 月在荷兰通过全国社区测试获得的具有已知免疫状态的个体的 1 份测序 SARS-CoV-1.617.2 样本。他们发现证据表明“Beta (B.1.1.7)、Gamma ( P.14) 或 Delta (B.59) 变体与接种疫苗后的 Alpha (B.60) 变体相比。 疫苗之间没有发现明显差异。 然而,与 XNUMX 天或更长时间相比,在完全接种疫苗后的前 XNUMX-XNUMX 天内效果更大。 与疫苗诱导的免疫力相反,在具有感染诱导的免疫力的个体中,与 Alpha 变异体相比,没有发现再次感染 Beta、Gamma 或 Delta 变异体的风险增加。” |
| 31) 迪福斯科等人。 | 迪富斯科等人。 对完全接种 BNT19b162 疫苗的免疫功能低下患者的 COVID-2 疫苗突破性感染进行了评估。 “在完全接种疫苗(第 19 剂后≥14 天)的 IC 个体(IC 队列)、2 个相互排斥的 IC 条件组和一个非 IC 队列中检查了 COVID-12 疫苗突破性感染。” 他们发现,“在接受 1,277,747 剂 BNT16b2 的 162 名年龄≥2 岁的个体中,有 225,796 人 (17.7%) 被确定为 IC(中位年龄:58 岁;56.3% 为女性)。 最普遍的 IC 病症是实体恶性肿瘤 (32.0%)、肾脏疾病 (19.5%) 和风湿病/炎症病症 (16.7%)。 在完全接种疫苗的 IC 和非 IC 队列中,研究期间共观察到 978 例突破性感染; 124 例 (12.7%) 住院,2 例 (0.2%) 住院死亡。 IC个人占比38.2%(N = 374) 在所有突破性感染中,59.7% (N = 74) 的所有住院治疗,以及 100% (N = 2) 住院患者死亡。 IC 队列中突破性感染的比例是非 IC 队列的 3 倍(N = 374 [0.18%] 对比 N = 604 [0.06%]; 未经调整的发病率分别为每 0.89 人年 0.34 和 100。” |
| 32) 马拉帕蒂 (自然) | (《自然》杂志)报道说,如果你已经感染了疫苗,接种疫苗的保护作用“相对较小,并且在接种第二针后三个月内会惊人地减少”。 马拉帕蒂进一步补充说,我们一直在警告公共卫生界,即感染 Delta 的人鼻子中的病毒遗传物质水平大致相同,“无论他们以前是否接种过疫苗,这表明接种过疫苗和未接种过疫苗的人可能同样具有传染性。” Mallapaty 报告了在 139,164 年 95,716 月至 2 年 2021 月期间,英国 XNUMX 名感染 SARS-CoV-XNUMX 的人的 XNUMX 名密切接触者的测试数据,当时 Alpha 和 Delta 变体正在争夺主导地位。 研究结果是“尽管疫苗确实提供了一些针对感染和继续传播的保护,但 Delta 抑制了这种影响。 一个人完全接种了疫苗,然后有一个'突破' Delta 感染传播病毒的可能性几乎是 Alpha 感染者的两倍。 此外,由 Delta 引起的突破性感染风险比由 Alpha 引起的感染风险更高。” |
| 33) 嘉等人。 | 嘉等。 据报道,PCR 循环阈值 (Ct) 值“在诊断时接种疫苗组和未接种疫苗组之间相似,但接种疫苗的个体病毒载量下降得更快。 在接种疫苗的患者中观察到抗刺突蛋白抗体的早期强烈增强,但是,与野生型疫苗株相比,这些针对 B.1.617.2 的滴度明显较低。” |
| 34) 威廉等人。 | 威廉等人。 报道了疫苗血清和单克隆抗体对 SARS-CoV-2 omicron 变体的中和作用降低。 “细胞/组织 使用真实 SARS-CoV-2 变体的研究结果表明,与目前流行的 Delta 变体相比,疫苗引发的血清对 Omicron 的中和功效严重降低,突出了 T 细胞介导的免疫是预防严重 COVID-19 的基本屏障。” |
| 35) 疾控中心报告 | CDC 报告了 43 例由 Omicron 变体引起的 COVID-19 病例的详细信息。 他们发现,“34 (79%) 发生在症状出现或收到 SARS-CoV-19 检测结果阳性前至少 14 天完成 FDA 授权或批准的 COVID-2 疫苗初级系列的人中。” |
| 36) Dejnirattisai 等人。 | Dejnirattisai 等人。 展示了针对 SARS-CoV-2 Omicron 变体的活中和滴度,并检查了它与针对 Victoria、Beta 和 Delta 变体的中和作用的关系。 他们报告说,“AZD1222 和 BNT16b2 初级课程的接受者的中和效价显着下降,有证据表明一些接受者根本无法中和。” |
| 37) 塞勒等人。 | 策勒等人。 评估了 Omicron 变体是否逃脱了抗体中和“由辉瑞 BNT162b2 mRNA 疫苗在仅接种疫苗或接种疫苗且先前感染的人群中引发”。 他们报告说,Omicron 变体“仍然需要 ACE2 受体才能感染,但能广泛逃避辉瑞引发的中和作用。” |
| 38) 霍尔姆汉森等人. | Holm Hansen 等人在丹麦的研究考察了接种两剂或加强剂 BNT2b162 或 mRNA-2 疫苗系列后 Omicron 或 Delta 变体对 SARS-CoV-1273 感染的疫苗有效性。 据报道,一项关键发现是“在初次接种 BNT55.2b162 疫苗后,针对 Omicron 的 VE 最初为 2%,但此后迅速下降。 尽管估计精度较低,但在初级 mRNA-1273 疫苗接种后针对 Omicron 的 VE 同样表明保护迅速下降。 相比之下,这两种疫苗都显示出对 Delta 的更高、更持久的保护。” 换句话说,对 Delta 失败的疫苗对 Omicron 来说更糟糕。 下表和下图描绘了一幅毁灭性的画面。 查看垂直线中绿点(Omicron 变体)的位置(蓝色是 Delta)和条形的 2 个边缘(上唇和下唇)Omicron 91 天(3 个月)。 辉瑞和 Moderna 在 31 天时都显示出对 Omicron 的负面疗效(均低于“无效线”或“0”)。 比较表更具破坏性,因为它显示了 Omicron 的疫苗有效性要低得多。 例如,在 1-30 天,辉瑞显示 Omicron 的有效性为 55.2%,而 Delta 的有效性为 86.7%,而在同一时期,Moderna 显示 Omicron 的有效性为 36.7%,而 Delta 的有效性为 88.2%。 |
| 39) 英国卫生安全局 | 英国报告显示,助推器可预防由 Omicron 引起的有症状的 COVID-19 约 10 周; 这 英国卫生安全局 据报道,对于那些最初接种辉瑞与 BioNTech 开发的疫苗的人,在辉瑞加强剂后,对由该变体引起的症状性 COVID-19 的保护从 70% 下降到 45%。 专门报道的 英国卫生安全局 显示“在接受阿斯利康初级课程的人中,疫苗有效性在辉瑞或 Moderna 加强剂后 60 至 2 周后约为 4%,然后在辉瑞加强剂和 Moderna 加强剂后 35 周降至 45% 和 10%。助推器。 在接受辉瑞初级课程的人中,辉瑞加强剂后的疫苗有效性约为 70%,45 多周后降至 10%,而 Moderna 加强剂后长达 70 周,疫苗有效性保持在 75% 至 9% 左右。” |
| 40) 布坎等人. | 巴肯等人。 在 22 年 19 月 2021 日和 2 月 19 日期间使用测试阴性设计来评估针对 OMICRON 或 DELTA 变体的疫苗有效性(无论症状或严重程度如何)。他们包括至少接受过 1 剂 COVID-3,442 疫苗的人(其中至少有 9,201 剂初级系列的 mRNA 疫苗剂量),并应用多变量逻辑回归建模分析来“从最近一剂开始按时间估计两剂或三剂的有效性。” 其中包括 471,545 例 Omicron 阳性病例、2 例 Delta 阳性病例和 93 例检测阴性对照。 接种 95 剂后,“针对 Delta 感染的疫苗有效性随着时间的推移稳步下降,但在接受第三剂 mRNA 疫苗后 ≥92 天恢复至 94%(7%CI,2-19%)。 相比之下,接受 37 剂 COVID-95 疫苗对 Omicron 没有保护作用。 在接受第三剂 mRNA 疫苗后 ≥ 19 天,针对 Omicron 的疫苗有效性为 50%(7%CI,XNUMX-XNUMX%)。” |
| 41) 苏格兰公共卫生 COVID-19 和冬季统计报告 | Public Health Scotland COVID-19 & Winter Statistical Report(出版日期:19 年 2022 月 38 日)在第 44 页(病例率)、第 50 页(住院)和第 2 页(死亡)中提供了惊人的数据,表明疫苗接种失败了 Delta 但至关重要的是,omicron 失败了。 XNUMXnd 接种数据尤其值得关注。 表 14 年龄标准化病例数据非常令人不安,因为它在多周的研究中显示,在每个剂量(1 对 2 对 3 次加强接种)中,接种疫苗的人比未接种疫苗的人感染率高得多,其中 2nd 剂量惊人地升高(见灰色行)。 2 岁后急性住院的年龄标准化率惊人地升高nd 2022 年 16 月期间接种(超过未接种疫苗者)。查看表 19,该表按疫苗接种状态报告了与 COVID-2 相关的确诊死亡人数,我们再次观察到 XNUMXnd接种。 该数据向我们表明,该疫苗与感染有关,并且对 omicron 的作用并非最佳,而且保护作用有限,而且迅速减弱。 |
| 42) 英国的 COVID-19 疫苗监测报告第 3 周,20 年 2022 月 XNUMX 日 | 英国 19 年 3 月 20 日第 2022 周的 COVID-9 疫苗监测报告引起了人们对 Delta(现在基本上被 omicron 占据主导地位)和 omicron 疫苗失败的严重关切。 当我们查看第 34 页表 19(51 年第 2021 周至 2 年第 2022 周期间按疫苗接种状态分类的 COVID-2 病例)时,我们发现第 XNUMX 周的病例数更多nd 4th 和5th 轴车削中心rd 接种。 第 38 页的重要表格,图 12(接种疫苗和未接种疫苗人群的 COVID-19 感染率、住院率和死亡率未经调整)向我们展示了过去 2 至 3 至 4 个月英国数据的持续模式,目前的报告表明收到 3rd 与未接种疫苗的人(30 岁及以上年龄层)相比,接种疫苗(助推器)的感染/病例风险要大得多。 |
| 43) 英国公共卫生监测报告 | 在最近的英国公共卫生监测报告中 9周, 8周, 以及第 7 周 (英国 COVID-19 疫苗监测报告第 7 周 17 年 2022 月 XNUMX 日), 第 6 周 (COVID-19 疫苗监测报告 第 6 周 10 年 2022 月 XNUMX 日) 和 5 年的第 2022 周 (COVID-19 疫苗监测报告 第 5 周 3 年 2022 月 XNUMX 日) 以及自疫苗推出以来 2021 年积累的报告,我们看到接种疫苗的人感染风险更高,尤其是 18 岁以上的年龄组,以及住院甚至死亡的风险。 这对于那些接受双重疫苗接种的人来说尤其明显。 接种三联疫苗的人死亡风险增加,尤其是随着年龄的增长。 同样的模式出现在苏格兰的数据中。 |
| 44)。 Regev-Yochay 等人。 | Regev-Yochay 等人。 在以色列 看过(发表日期16月XNUMX日th 2022)第四剂的免疫原性和安全性(4th) BNT162b2 (Pfizer–BioNTech) 或 mRNA-1273 (Moderna) 在第三剂后 4 个月在一系列三剂 BNT162b2 中给药)。 这是一项开放标签、非随机临床研究,评估了 4th 剂量方面的需要超过 3rd 剂量。 在参加 Sheba HCW COVID-1050 队列的 '19 名合格医护人员中,154 人接受了第四剂 BNT162b2,1 周后,120 人接受了 mRNA-1273。 对于每个参与者,从其余符合条件的参与者中选择两个年龄匹配的对照。 研究人员进一步报告说,“总体而言,对照组中有 25.0% 的参与者感染了 omicron 变体,而 BNT18.3b162 组的参与者和 mRNA-2 组的参与者分别为 20.7% 和 1273%。 BNT2b30 对任何 SARS-CoV-95 感染的疫苗效力为 9%(55% 置信区间 [CI],-162 至 2),mRNA-11 为 95%(43% CI,-44 至 1273)......受感染的参与者具有潜在的传染性,病毒载量相对较高(核衣壳基因周期阈值,≤25)'。 结果表明,mRNA 疫苗的最大免疫原性在三剂后达到。 更具体地说,研究人员“观察到疫苗对医护人员感染的效力较低,而病毒载量相对较高,这表明被感染的人具有传染性。 因此,对健康的年轻卫生保健工作者进行第四次疫苗接种可能只会带来微不足道的好处”。 |
| 45)。 安德鲁斯等人。 | 安德鲁斯等人。 使用测试阴性病例对照设计来估计疫苗对英国 omicron 和 delta (B.1.617.2) 变体引起的症状性疾病的有效性。 “在用两剂 BNT162b2 (Pfizer-BioNTech)、ChAdOx1 nCoV-19 (AstraZeneca) 或 mRNA-1273 (Moderna) 疫苗进行初次免疫后,以及在加强剂量的 BNT162b2、ChAdOx1 nCoV-19 或 mRNA 后计算疫苗有效性-1273。” 结果表明,使用两剂 ChAdOx1 nCoV-19 或 BNT162b2 疫苗进行免疫对 omicron 变体引起的症状性疾病提供的保护非常有限。 “在 ChAdOx162 nCoV-2 或 BNT1273b1 初级课程之后的 BNT19b162 或 mRNA-2 助推器显着增加了保护,但这种保护随着时间的推移而减弱。” |
| 46) 霍夫曼等人。 | 霍夫曼等人。 发表在 CELL 杂志上的 OMICRON 刺突蛋白(抗原)逃避了来自“恢复期患者或接种了 BioNTech-Pfizer 疫苗(BNT162b2)的个体的抗体的中和,其效率比 Delta 变体的刺突蛋白高 12 至 44 倍。 异源 ChAdOx1(Astra Zeneca-Oxford)/BNT162b2 疫苗接种或接种三剂 BNT162b2 后诱导的抗体对 Omicron 刺突的中和更有效,但 Omicron 刺突仍然比 Delta 刺突更有效地逃避中和。” 总体而言,结果表明大多数治疗性抗体对 Omicron 变体无效,令人担忧的是,BNT162b2(辉瑞)的双重接种可能无法“充分预防由该变体引起的严重疾病”。 |
| 47) 酒吧等。 | Bar-on 等人。 在 NEJM 上发表,标题为: 第四剂 BNT162b2 对以色列 Omicron 的保护作用. 他们评估了以色列卫生部的数据库,并在 SARS-CoV-1,252,331 的 B.60(微米)变体被感染期间挑选了 1.1.529 名 2 岁或以上且有资格接受第四剂疫苗的人的数据。主要(10 年 2 月 2022 日至 19 月 8 日)。 分析的重点是确诊感染率和严重 Covid-3 与时间的函数关系,从接受第四剂(四剂组)后 7 天开始,与仅接受三剂(三剂组)的人相比剂量组)和在 XNUMX 至 XNUMX 天前接受第四剂的人(内部对照组)。 他们采用了准泊松回归模型并调整了混杂因素,据报道调整了年龄、性别、人口统计组和日历日。 主要调查结果强调了 4th 剂量,如下:“比较自第四次剂量以来随时间变化的比率(图2) 表明 omicron 变体对确诊感染的保护作用在接种疫苗后的第四周达到最大值,之后到第八周,比率下降到大约 1.1; 这些发现表明,对确诊感染的保护作用迅速减弱……第四剂后第 1.1 周调整后的感染率与对照组非常相似; 三剂组与四剂组的比率为95(1.0% CI,1.2~1.0),内对照组与四剂组的比率仅为95( 0.9% CI,1.1 到 XNUMX)。” 这些发现表明没有区别。 我们也对该方法感到担忧,因为很明显他们无法或没有控制可能影响调查结果的紧迫混杂(扭曲)变量。 这通常会导致高估(或低估)治疗效果。 例如,他们是否控制了先前的感染,他们是否控制了早期治疗药物的使用,他们是否调整了第 4 剂量组的行为差异,或预先存在的条件,或差异治疗等。研究人员确实考虑了一些偏见,例如“这些潜在的偏见包括‘健康的疫苗接种者’偏见,在这种偏见中,感觉不适的人往往不会在接下来的几天内接种疫苗,这导致四剂疫苗组在第一天的确诊感染和严重疾病数量减少接种疫苗后。 此外,人们预计由于行为变化导致的检测偏差,例如在接种疫苗后进行较少测试的趋势,在接受剂量后不久就会更加明显。” |
| 48) 美国大型卫生系统中由于 omicron 和 delta 变体导致 BNT162b2 疫苗对医院和急诊科入院的持久性:一项测试阴性病例对照研究,塔尔托夫,2022 年。 | 研究人员评估了两剂和三剂 BNT162b2 (Pfizer–BioNTech) mRNA 疫苗对因 delta (B.1.617.2) 和 omicron 变异而住院和急诊的有效性和持久性; 一项采用阴性试验设计的病例对照研究,分析 电子健康记录 1 年 2021 月 6 日至 2022 年 11 月 123 日期间,美国加利福尼亚州的一个大型综合卫生系统 Kaiser Permanente Southern California (KPSC) 的成员; “对 162 名医院或急诊科入院患者进行了分析。 在调整后的分析中,两剂 BNT2b41 疫苗针对 omicron 变体的入院效果分别为 95% (21% CI 55-31) 和 16% (43-9) 在第二次后 3 个月或更长时间入院时剂量”; 研 |
| 49) Laith J. Abu-Raddad 等人。 (2022 年 XNUMX 月): | “mRNA 疫苗助推器对卡塔尔 SARS-CoV-2 Omicron 感染的影响”; 如我们所见,疫苗失败,VE <50%(所需阈值)和“0”死亡; “两项匹配的回顾性队列研究评估了加强疫苗接种的有效性,与单独的两剂初级系列相比,在大波 omicron 期间对有症状的 SARS-CoV-2 感染和 Covid-19 相关住院和死亡的影响从 19 年 2021 月 26 日到 2022 年 50 月 0 日的感染。使用 Cox 比例风险回归模型估计了加强状态与感染的关联。” 正如我们所见,疫苗失败了,VE <XNUMX%(所需阈值)和“XNUMX”死亡。 主要调查结果如下,表明疫苗未达到 50% 的有效性阈值: BNT162b2 Booster 对 Omicron 变体的有效性 “与两剂主要系列相比,BNT162b2 加强剂(辉瑞)对症状性 omicron 感染的估计有效性为 49.4%(95% CI,47.1 至 51.6)。” mRNA-1273 Booster 对 Omicron 变体的有效性 “与两剂初级系列相比,mRNA-1273 加强剂 (Moderna) 的估计有效性为 47.3% (95% CI, 40.7 至 53.3)。” 其他分析 “对于 BNT162b2 疫苗分析,在加强接种后第 15 天开始随访,与两剂初次系列相比,加强对症状性 omicron 感染的估计有效性为 49.9%( 95% CI,47.6 至 52.2)(图 S2 和表 S4)。 mRNA-1273 疫苗的相应估计有效性为 52.0%(95% CI,45.1 至 57.9)。 两种有效性估计都与主要分析中的相似。 在第二次接种后 162 个月或更短时间接受加强免疫的人群中,与两剂主要系列相比,BNT2b38.0 疫苗加强免疫对症状性 omicron 感染的估计有效性为 95%(28.8% CI,46.0 至 8)在第二剂后超过 50.5 个月接受的患者中,剂量和 95%(48.2% CI,52.8 至 8)。 mRNA-1273 疫苗有效性的相应估计值为 41.5%(95% CI,32.3 至 49.5)和 56.8%(95% CI,47.0 至 64.8)。 |
| 50) 弗莱明-杜特拉等人。 | 弗莱明杜特拉等。 检查了 先前 BNT162b2 COVID-19 疫苗接种与 Omicron 优势期间儿童和青少年症状性 SARS-CoV-2 感染的关联. 他们用 2021 年 2022 月至 121 年 952 月在 Omicron 变异优势期间进行的一项测试阴性病例对照研究,包括来自美国各地的 5 11 次测试,估计 60.1 至 2 岁儿童的疫苗对症状感染的有效性为 4% 2 至第 28.9 剂后 2 周和第 2 剂后第 12 个月期间为 15%。在 59.5 至 2 岁的青少年中,估计疫苗有效率在第 4 剂后 2 至 16.6 周为 2%,在第 2 个月期间为 2%(见图 162)。 他们得出的结论是,“在儿童和青少年中,估计 2 剂 BNT0b4.5 针对症状性感染的疫苗有效性迅速下降”。 我们看到 VE 在大约 XNUMX 个月时跌至 XNUMX 以下。 |
| 51) 拉索尼埃 等: | Lassaunière 等人: “在第二次和第三次 BNT2b1 mRNA 疫苗接种后 1 至 18 周,中和针对 SARS-CoV-162 Omicron 变体 (BA.2) 的抗体”; “我们的研究发现,仅在第二次和第三次 BNT162b2 给药几周后,Omicron 特异性血清中和抗体滴度迅速下降……观察到的群体中和抗体滴度下降对应于疫苗针对聚合酶链反应的效力下降——已确认丹麦的 Omicron 感染和英国的有症状的 Omicron 感染……总的来说,第二和第三剂 BNT162b2 后疫苗诱导的保护性抗体反应是短暂的,可能需要额外的加强剂量,特别是在老年人中; 然而,保守的 T 细胞免疫和非中和抗体仍可提供免于住院和死亡的保护。” |
| 52) 对 SARS-CoV-2 的天然和混合免疫的保护和减弱 | “每 2 人日的 SARS-CoV-100,000 感染病例数(调整后的感染率)随着接种 BNT162b2 疫苗或上次感染后的时间增加而增加。 在从感染中恢复的未接种疫苗的人中,这一比率从感染 10.5 个月至不到 4 个月的人中的 6 增加到感染 30.2 年或更长时间的人中的 1。 在先前感染后接种单剂疫苗的人群中,接种时间少于 3.7 个月的调整后比率较低(2),但在至少 11.6 个月前接种疫苗的人群中增加到 6。 在接种过两剂疫苗的先前未感染者中,调整后的比率从接种不足 21.1 个月的人群中的 2 增加到接种至少 88.9 个月的人群中的 6。 在先前感染过 SARS-CoV-2 的人中(无论他们是否接种过任何剂量的疫苗,或者是否在感染之前或之后接种过一剂疫苗),随着自最后一次免疫后时间的增加,对再感染的保护会降低——授予活动; 但是,这种保护高于以前未感染者接种第二剂疫苗后相同时间后所赋予的保护。 感染后的单剂疫苗加强了对再感染的保护。” |
| 53) CDC 和 mRNA 疫苗在 Delta 和 Omicron 变体占主导地位期间针对 COVID-2 相关的急诊科和紧急护理遭遇和住院治疗的 3 剂和 19 剂疫苗有效性减弱 — VISION 网络,10 个州,2021 年 2022 月至 2022 年 XNUMX 月,费迪南德,XNUMX: | “在 Omicron 主导时期,与 Delta 主导时期相比,针对 COVID-19 相关 ED/UC 遭遇的 VE 总体较低,并且在第二次接种后减弱,从接种疫苗后 69 个月内的 2% 降至 37%接种后 ≥ 5 个月 (p<0.001)。 第三剂后保护作用增强,过去 87 个月内接种疫苗的人的 VE 为 2%; 然而,在 3-66 个月前接种疫苗的人中,接种 4 剂后的 VE 下降到 5%,在 ≥31 个月前接种疫苗的人中下降到 5%”……在对 241,204 次 ED/UC 遭遇和 93,408 次住院的 COVID-19 成人患者的多态分析中与 26 年 2021 月 22 日至 2022 年 19 月 XNUMX 日期间的疾病一样,在 Omicron 占主导时期,VE 对实验室确认的 COVID-XNUMX 的估计值低于 Delta 占主导时期,在考虑了接受的疫苗剂量和自接种疫苗的时间之后接种疫苗。 在这两个时期,接受第三剂后的 VE 总是高于接受第二剂后的 VE; 然而,VE 随着接种疫苗后时间的增加而减弱。” |
| 54) 初级计划和初始加强疫苗全面接种后的严重 COVID-19 结果:对英格兰、北爱尔兰、苏格兰和威尔士 30 万人的国家前瞻性队列研究的汇总分析, Agrawal 等人,2022 年 XNUMX 月 | “在完成 BNT19b10 或 ChAdOx162 nCoV-2 的主要剂量(≥1 周)后 19 周,出现严重 COVID-20 结果的风险增加 vs 3-9 周; aRR 4·55 [95% CI 4·16–4·99])。 合并症较多的个体(≥5 种合并症 vs 没有任何; 7·98 [7·73–8·24],年龄较大(≥80岁) vs 18-49岁; 8·12 [7·89–8·35]),BMI 较高(≥40 vs 18·5–24·9; 1·75 [1·69–1·82]),或男性(男性 vs 女性; 1·19 [1·17–1·21]) 也与严重 COVID-19 结果的风险增加有关。” 这项在英国范围内对超过 16 万人进行的基于人口的调查 英格兰、北爱尔兰、苏格兰和威尔士 已经发现,在第一次加强疫苗接种后,老年人、多发病率高的人和具有某些潜在健康状况的人仍然面临与 COVID-19 相关的住院和死亡的最高风险。 这些发现对于疫苗倡导者来说是非常成问题的。 COVID 基因注射疫苗失败,没有杀菌、没有中和作用,不能保护上呼吸道(不能防止感染或传播),也不能有效或适当地保护下肺免受严重疾病的侵害。 |
| 55) 减少第一剂和第二剂 ChAdOx1 和 BNT162b2 COVID-19 疫苗接种:一项针对英格兰、北爱尔兰、苏格兰和威尔士的 12.9 万人的汇总目标试验研究, 可儿, 2022 | “对于 ChAdOx1 的第 2 剂和第 1 剂以及 BNT1b162 的第 2 剂,VE/rVE 在大约第 60-80 天达到零,然后变为负数。 到第 70 天,对于 ChAdOx25 的第 95 剂和第 80 剂,VE/rVE 分别为 -14%(10% CI:-95 至 32)和 39%(1% CI:-2 至 1)和 42%(95% BNT9b64 的第 53 剂和第 95 剂分别为 CI:26 至 70)和 1%(2% CI:162 至 2)。 BNT2b162 剂量 2 的 rVE 始终保持在零以上,并在 46 天的随访后达到 95%(13% CI:67 至 98)。 发现有力的证据表明 ChAdOx1 的第 2 剂和第 1 剂以及 BNT1b162 的第 2 剂的 VE/rVE 减弱。” 这些发现对公共卫生当局来说并不陌生。 实际上, 疾病预防控制中心主任罗谢尔·瓦伦斯基 曾表示,Covid 疫苗对严重疾病和死亡的效果“非常好”,但“它们不能再做的是防止传播。” 这些研究表明,疫苗对于减少严重疾病和死亡很重要,但无法防止疾病传播并最终感染我们大多数人。 也就是说,虽然疫苗为被接种者,特别是对老年高危人群提供了个人利益,但普遍接种疫苗的公共利益却受到严重质疑。 因此,不应期望 Covid 疫苗有助于消除病毒的社区传播或实现群体免疫。 这揭示了疫苗授权和护照的基本原理。 |
| 56)。 第四次 BNT162b2 疫苗剂量后六个月的随访, 卡内蒂 & Regev-Yochay, 2022 | “在之前没有感染过 SARS-CoV-2 的参与者中,6113 人被纳入体液反应分析,11,176 人被纳入疫苗有效性分析(图 S1 和表 S2 和 S3)。 抗体反应在大约 4 周时达到峰值,到 13 周时减弱到第四次给药前的水平,然后稳定下来。 在整个 6 个月的随访期间,接受第三剂和第四剂后调整后的每周 IgG 和中和抗体水平相似,并且明显高于接受第二剂后的水平(图1A和1B 和表 S4)。 累积发病率曲线如图S2,疫苗有效性如图SXNUMX所示 图1C. 与接受三剂疫苗(至少在 162 个月前接受第三剂)相比,接受第四剂 BNT2b2 疫苗对 SARS-CoV-4 感染提供了更多保护(总体疫苗有效性,41%; 95% 置信区间 [CI],35 至 47)。 特定时间的疫苗有效性(在我们的分析中,比较了接种疫苗后尚未感染的参与者的感染率)随着时间的推移而减弱,在接种疫苗后的前 52 周内从 95%(45% CI,58 至 5)下降在 2 至 95 周时降至 -27%(17% CI,-15 至 26)。” 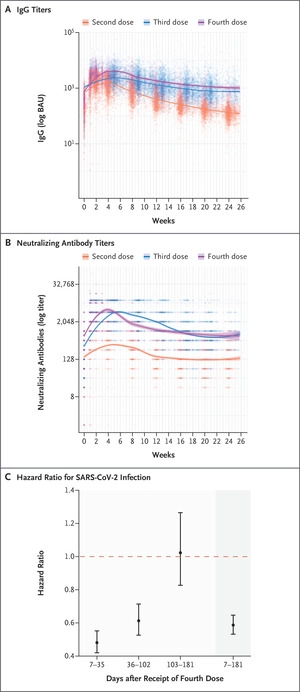 |
| 57) mRNA-1273 对 SARS-CoV-2 omicron 和 delta 变体的有效性, 曾, 2022 | “在 2-14 天时,针对 omicron 感染的 90 剂 VE 为 44.0%(95% CI,35.1-51.6%),但下降很快。 3 剂 VE 对 delta 感染的预防率为 93.7% (92.2–94.9%) 和 86.0% (78.1–91.1%),对 omicron 感染的预防率为 71.6% (69.7–73.4%) 和 47.4% (40.5–53.5%) 在 14-分别为 60 天和 >60 天。 在免疫功能低下的个体中,3 剂 VE 对 omicron 感染的抑制率为 29.4%(0.3–50.0%)。 使用 delta 或 omicron 的 3 剂 VE 对住院治疗的影响 > 99%。 我们的研究结果表明 3 剂量 VE 对 delta 感染具有高效、持久的作用,但对 omicron 感染的有效性较低,尤其是在免疫功能低下的人群中。 然而,3 剂量 VE 对 delta 或 omicron 的住院治疗效果显着。” |
| 58) 冰岛 Omicron 波期间 SARS-CoV-2 再感染率, 埃索尔松, 2022 | “包括 11 536 名 PCR 阳性者。 平均 (SD) 年龄为 34 (19) 岁(中位数,31 岁;范围,0-102 岁),5888 人 (51%) 为男性,2942 人 (25.5%) 至少接种过 1 剂疫苗,并且从初次感染开始的平均 (SD) 时间为 287 (191) 天(中位数,227 天;范围,60-642 天); 再感染的可能性随着初次感染时间的推移而增加(18 个月 vs 3 个月的比值比,1.56;95% CI,1.18-2.08)(数字) 并且在接种 2 剂或更多剂疫苗的人中高于接种 1 剂或更少疫苗的人(比值比,1.42;95% CI,1.13-1.78)” |
| 59) mRNA-1273 对 SARSCoV-19 Omicron 亚变体感染和 COVID-2 住院治疗的有效性:BA.1、BA.2、BA.2.12.1、BA.4 和 BA.5, 曾, 2022 | “虽然针对 BA.3 感染的 1 剂 VE 较高且缓慢下降,但针对 BA.2、BA.2.12.1、BA.4 和 BA.5 感染的 VE 最初为中度至高度 (61.0%-90.6% 14第三剂后 -30 天)并迅速消退。 针对 BA.4、BA.2 和 BA.2.12.1 感染的 4 剂 VE 在 64.3%-75.7% 之间,并且在第四剂后 30.8-5 天针对 BA.14 的 VE 较低 (30%),消失所有子变体都超过 90 天。” |
| 60) COVID-19 疫苗在 13 个月内的有效性,涵盖瑞典人口中出现 Omicron 变体的时期, 于, 2022 | “在 Omicron 之前,两剂疫苗显示出持久的良好抗感染保护作用(所有时间间隔内的 VE 均高于 85%),但对 Omicron 感染的保护作用较弱(到第 43 周下降到 14%,到第 80 周时没有保护作用)。 同样,在 Omicron 之前,针对住院的 VE 很高且稳定,但在 Omicron 期间明显减弱,尽管 VE 估计值(到第 25 周时高于 40%,到第 40 周时下降到 XNUMX%)远高于抗感染。” |
| 61) 通过感染史和临床易感性和免疫印迹的长期 COVID-19 助推器有效性, 切迈特利, 2022 | “与初级系列相比,增强剂在一年内对感染的有效性为 41.1%(95% CI:40.0-42.1%),对严重、危重或致命的 COVID-80.5 的有效性为 95%(55.7% CI:91.4-19%)加强后的后续工作。 在临床上易感染严重 COVID-19 的人群中,对感染的有效性为 49.7%(95% CI:47.8-51.6%),对严重、危重或致命 COVID-84.2 的有效性为 95%(58.8% CI:93.9-19%)。 在加强后的第一个月,抗感染的有效性最高为 57.1%(95% CI:55.9-58.3%),但此后逐渐减弱,到第六个月时仅为 14.4%(95% CI:7.3-20.9%)。 在第 4 个月及之后,与 BA.5/BA.2.75 和 BA.20.3* 亚变异发生率一致,有效性在一年的随访后逐渐下降至 -95%(55.0% CI:-29.0-162%) . 无论先前的感染状态、临床易感性或疫苗类型如何(BNT2b1273 与 mRNA-XNUMX),都观察到了相似的保护水平和模式。”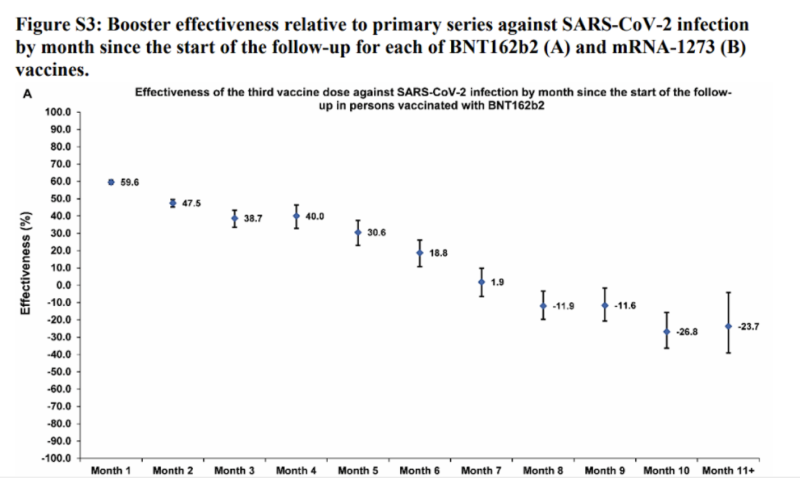 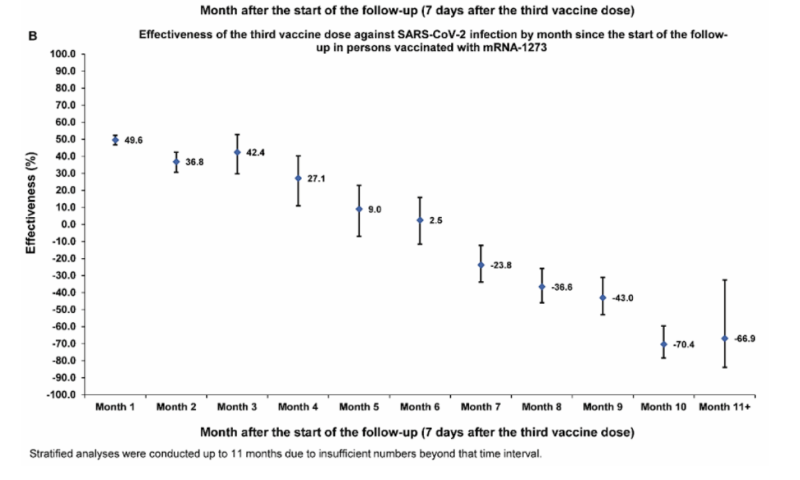 |
| 62) SARS-CoV-2 BQ 和 XBB 亚变体上升的抗体逃避特性令人担忧, 王, 2022 | “BQ.1、BQ.1.1、XBB 和 XBB.1 是迄今为止抵抗力最强的 SARS-CoV-2 变体; 血清中和作用显着降低,包括二价加强剂; 所有临床单克隆抗体都对这些变体失去活性; 这些变体的 ACE2 亲和力与其亲本菌株相似; SARS-CoV-2 Omicron 的 BQ 和 XBB 亚变体现在正在迅速扩展,这可能是由于它们的额外刺突突变导致抗体逃避特性发生了改变。 在这里,我们报告说,来自疫苗接种者和感染者的血清对 BQ.1、BQ.1.1、XBB 和 XBB.1 的中和作用明显受损,包括来自使用 WA1/BA.5 双价 mRNA 疫苗加强的个体的血清。 针对 BQ 和 XBB 亚变体的滴度分别降低了 13-81 倍和 66-155 倍,远远超出迄今为止观察到的水平。 能够中和原始 Omicron 变体的单克隆抗体对这些新的亚变体基本上没有活性,并且确定了负责的个体刺突突变。 发现这些亚变体与其前身具有相似的 ACE2 结合亲和力。 总之,我们的研究结果表明,BQ 和 XBB 亚变体对当前的 COVID-19 疫苗构成严重威胁,使所有授权抗体失去活性,并且可能由于它们在逃避抗体方面的优势而在人群中占据主导地位。” |
| 63) 亲本 mRNA 疫苗或 BA.2-二价加强剂对 SARS-CoV-2.75.2 Omicron BA.1.1、BQ.1 和 XBB.5 的低中和作用, 库尔哈德, 2022 | “新出现的 SARS-CoV-2 Omicron 亚系,包括 BA.2 衍生的 BA.2.75.2 和 BA.5 衍生的 BQ.1.1 和 XBB.1,已经积累了可能影响疫苗有效性的额外刺突突变。 在这里,我们报告了从个体中收集的三个人血清组的中和活性,这些个体在第 23 剂亲本 mRNA 疫苗后 94-4 天,在 BA.14-二价加强剂后 32-5 天从具有 2-4 剂亲本 mRNA 的个体中收集疫苗,或从先前感染过 SARS-CoV-15 的个体接种 BA.32-二价加强剂和 5-2 剂亲本 mRNA 疫苗后 2-4 天。 结果表明,在加强后 5 至 4 天测量的 BA.5-二价加强剂引发了针对 BA.14/32 的高中和效价; 然而,BA.5-bivalent-booster 没有对新出现的 BA.2.75.2、BQ.1.1 或 XBB.1 产生强大的中和作用。 以前的感染显着增强了 BA.5-二价助推器引发的中和作用的幅度和广度。 我们的数据支持一种疫苗更新策略,即未来的助推器应该与新出现的循环 SARS-CoV-2 变体相匹配。” |
| 64) 2019 年冠状病毒病 (COVID-19) 双价疫苗的有效性, 什雷斯塔, 2022 | “一项在美国克利夫兰诊所卫生系统 (CCHS) 进行的回顾性队列研究。 研究人员包括在二价 COVID-19 疫苗首次面世当天的员工。 “使用 Cox 比例风险回归评估疫苗接种提供的保护(分析为时间依赖性协变量)。” 调查结果集中在 51,011 名员工身上,其中 20,689 名 (41%) 有先前记录的 COVID-19 感染(发作),其中 42,064 名 (83%) 至少接种了两剂疫苗。 “根据俄亥俄州卫生部提供的 SARS-CoV-4 变体监测数据,在研究的前 5 周内,俄亥俄州的大多数感染是由 Omicron 变体的 BA.10 或 BA.2 谱系引起的。 到 1 月,BQ.1.1、BQ.7 和 BF.XNUMX 谱系占感染的很大一部分。 '到研究结束时,10804 人 (21%) 接受了二价疫苗加强接种。 二价疫苗是 9595 名(89%)的辉瑞疫苗和其余 1178 名的 Moderna 疫苗。总共有 2452 名员工(5%)在研究的 19 周内获得了 COVID-13。 “从该模型计算出的总体疫苗有效性为 30%(95% CI,20% – 39%)……当 Omicron BA.4/BA.5 谱系是主要的流行菌株时。” “多变量分析还发现,最近一次 COVID-19 发作的时间越近,患 COVID-19 的风险就越低,而之前接种的疫苗剂量越多,患 COVID-19 的风险就越高。” |
| 65) 与第一次加强剂相比,第二次加强剂的有效性以及先前 SARS CoV-2 感染对法国有症状的 Omicron BA.2 和 BA.4/5 的保护作用, 塔曼朱, 2023 | “我们纳入了 60 年 2 月 21 日至 30 月 2022 日期间接受过 SARSCoV-181 检测的有症状的 ≥210 岁个体。与 39-95 天大的第一次加强剂相比,第二次加强剂恢复了保护,有效性为 38% [41%CI: 7% – 30%],接种后 XNUMX-XNUMX 天,在接种疫苗后的相同时间点,这种保护增益低于第一次加强免疫时观察到的保护增益。” |
| 66) 延长 SARS-CoV-2 RBD 加强疫苗接种诱导小鼠体液和细胞免疫耐受, 高 2023 | i) 我们的研究结果表明持续使用 SARS-CoV-2 疫苗加强剂存在潜在风险,对全球 COVID-19 疫苗接种增强策略具有直接影响。 ii) 这种疫苗诱导的免疫反应的重建是否可以通过持续应用加强剂来重复,目前尚不清楚,但尚不清楚。 在这里,我们在 Balb/c 小鼠模型中比较了重复 RBD 疫苗加强剂与常规免疫课程与延长疫苗接种策略的效果。 iii) 我们发现,在延长的疫苗接种过程中,通过常规免疫建立的体液免疫和细胞免疫的保护作用均受到严重损害。 具体而言,延长疫苗接种不仅会完全削弱血清 RBD 特异性抗体的数量和中和功效,还会缩短长期体液记忆。 iv) 这与生发中心反应中的免疫耐受以及脾脏生发中心 B 和 Tfh 细胞数量减少有关。 此外,我们证明延长免疫降低了 CD4+ 和 CD8+ T 细胞的功能反应,抑制了记忆 T 细胞的数量,并上调了 Te 亚型细胞中 PD-1 和 LAG-3 的表达。 v) 还观察到 Treg 细胞的百分位增加,伴随着 IL-10 产量的显着升高。 我们共同提供了重要证据,证明重复接种 RBD 加强疫苗可能会对常规疫苗接种过程建立的免疫反应产生负面影响,并促进适应性免疫耐受。 vi) 继续接种疫苗促进了显着的适应性免疫耐受的形成,并严重损害了常规过程中已建立的免疫反应,抗原特异性抗体和 T 细胞反应的显着降低、免疫记忆的丧失和免疫抑制微环境的形成证明了这一点. |
| 67) 先前感染、疫苗接种和混合免疫对卡塔尔症状性 BA.1 和 BA.2 Omicron 感染和严重 COVID-19 的影响,阿尔塔拉奈,2022 年 XNUMX 月 | “卡塔尔研究人员在 2 年 1 月 2 日至 1 年 2 月 23 日期间调查了 SARS-CoV-2021 Omicron 症状性 BA.21 感染、症状性 BA.2022 感染、BA.6 住院和死亡以及 BA.162 住院和死亡。研究人员进行了 2 项全国性的、匹配的、测试阴性的病例对照研究,以检查 BNT1273b2 (Pfizer-BioNTech) 疫苗、mRNA-46.1 (Moderna) 疫苗、由于先前感染前 Omicron 变体而产生的自然免疫和混合免疫的有效性来自先前的感染和疫苗接种。 他们发现“仅先前感染对有症状的 BA.95 感染的有效性为 39.5%(51.9% CI:162-2%)。 仅接种两剂 BNT1.1b95 疫苗的有效性可忽略不计,为 -7.1%(4.6% CI:-162-2),但几乎所有个体都在几个月前接种了第二剂疫苗。 仅三剂 BNT52.2b95 疫苗接种的有效性为 48.1%(55.9% CI:162-2%)。 先前感染和两剂 BNT55.1b95 疫苗接种的混合免疫有效性为 50.9%(58.9% CI:1-2%)。” 关键发现是“针对 BA.XNUMX 和 BA.XNUMX 的先前感染、疫苗接种和混合免疫的影响没有明显差异。” |
| 68) 第四剂 mRNA COVID-19 疫苗对长期护理机构居民和高龄老人的全因死亡率的有效性:瑞典的一项全国性回顾性队列研究, 诺德斯特龙, 2022 | “从基线后 7 天起,LTCF 队列中有 1119 人死亡,中位随访时间为 77 天,最长随访时间为 126 天。 在第 7 至 60 天期间,第四剂的 VE 为 39%(95% CI,29-48),在第 27 至 95 天期间下降至 2%(48% CI,-61-126)。在所有年龄≥80 岁的个体中,有 5753 人在中位随访 73 天和最长随访 143 天期间死亡。 在第 7 至 60 天期间,第四剂的 VE 为 71%(95% CI,69-72),在第 54 至 95 天期间下降至 48%(60% CI,61-143)。” |
| 69) 第二剂 COVID-9 疫苗后长达 19 个月的感染、住院和死亡风险:瑞典的一项回顾性总人群队列研究, 诺德斯特龙, 2022 | “对于任何严重程度的 SARS-CoV-2 感染结果,BNT162b2 的疫苗有效性随着时间的推移逐渐减弱,在 92-95 天时从 92%(93% CI 0 到 001;p<15·30)下降到 47%( 39 到 55;p<0·001) 在第 121-180 天,从第 23 天起达到 2%(-41 到 0;p=07·211)。 mRNA-1273 的衰减稍慢,疫苗有效性在 96-94 天时为 97%(0 至 001;p<15·30),从第 59 天起为 18%(79 至 0;p=012·181) . 异源 ChAdOx1 nCoV-19 加 mRNA 疫苗的消退也稍慢,其疫苗有效性在 89-79 天时为 94%(0 至 001;p<15·30)和 66%(41 至 80;p<0 ·001) 从第 121 天开始。 相比之下,同源 ChAdOx1 nCoV-19 疫苗的疫苗有效性在 68-52 天时为 79%(0 至 001;p<15·30),从第 121 天起没有检测到有效性(-19% [-98 至 28] ;p=0·49)。 对于重症 COVID-19 的结果,疫苗有效性从第 89-82 天时的 93%(0 至 001;p<15·30)下降至第 64 天后的 44%(77 至 0;p<001·121)。 总的来说,有一些证据表明,男性的疫苗效力低于女性,老年人的疫苗效力低于年轻人。” |
| 70) 中和来自 mRNA Bivalent Booster 的 BA.2.75.2、BQ.1.1 和 XBB, 戴维斯-加德纳, 2023 | “在 VeroE6/TMPRSS2 细胞系中使用 FRNT1 比较从三个队列中的参与者获得的血清样本中的中和活性:第一个队列由 12 名参与者组成,在一次单价加强后 7 至 28 天; 第二,11 名参与者在第二次单价加强剂后 6 至 57 天; 第三,12 名参与者在二价助推器后 16 至 42 天。 在所有三个队列中,针对所有 omicron 亚变体的中和活性均低于针对 WA1/2020 菌株的中和活性; 针对 XBB 亚变体的中和活性最低(图1 和图 S2)。 在接受单价加强剂的队列中,FRNT50 GMT 对 WA857/1 为 2020,对 BA.60 为 1,对 BA.50 为 5,对 BA.23 为 2.75.2,对 BQ.19 为 1.1,并且低于对 XBB 的检测限。 在接受两个单价加强剂的队列中,FRNT50 GMT 对 WA2352/1 为 2020,对 BA.408 为 1,对 BA.250 为 5,对 BA.98 为 2.75.2,对 BQ.73 为 1.1,对 XBB 为 37。 这两个队列的结果对应于针对 BA.1 和 BA.5 的中和效价比针对 WA5/9 的中和效价低 1 至 2020 倍,针对 BA.2.75.2、BQ.1.1 和 XBB 的中和效价比针对 WA23/63 的中和效价低是 WA1/2020 的 XNUMX 到 XNUMX 倍。” |
| 71) SARS-CoV-2 Omicron 子变体 BA.2.12.1、BA.4 和 BA.5 的中和逃逸, 哈赫曼, 2022 | “在最初的两次 BNT162b2 免疫接种六个月后,针对 WA124/1 的中和抗体假病毒滴度中位数为 2020,但针对所有测试的 omicron 亚变体低于 20。 加强剂量给药两周后,中和抗体滴度显着增加,针对 WA5783/1 分离株为 2020,针对 BA.900 亚变体为 1,针对 BA.829 亚变体为 2,针对 BA.410 为 2.12.1子变体,以及 275 对 BA.4 或 BA.5 子变体。 在有 Covid-19 病史的参与者中,针对 WA11,050/1 分离株的中和抗体滴度中位数为 2020,针对 BA.1740 亚变体为 1,针对 BA.1910 亚变体为 2,针对 BA.1150 亚变体为 2.12.1 ,以及针对 BA.590 或 BA.4 子变体的 5。” |
发表于 知识共享署名4.0国际许可
如需转载,请将规范链接设置回原始链接 褐石研究所 文章和作者。









